(化学発光について手短に知りたい方は「(1)発光について」を飛ばして下の
「(2)化学発光について」を読んでください。)
(1)発光について
物質がエネルギーを吸収して光を出す現象を発光といい、そのエネルギー源として光、X線、熱、化学反応等があります。ここでは光をエネルギー源とする光発光を例にとり、その原理を説明します。
芳香族化合物などが光を吸収すると、光のエネルギー分だけエネルギーの高い状態になります。これを励起状態といいます。
光を吸収する前のエネルギーの低い安定な状態を基底状態といいます。 したがって、励起状態は余分なエネルギーをもっているために不安定な状態です。
物体を持ち上げると位置のエネルギー(ポテンシャルエネルギー)をもつために物体の支えをなくすと 物体はポテンシャルエネルギーの低い状態に戻ろうとして下に落ちます。
同じことは、光を吸収して励起状態になった化合物についてもいえます。エネルギーの高い励起状態から 余分のエネルギーを外部に放出して安定な基底状態になろうとします。このときのエネルギーの
放出の仕方には3通りあります。
1つ目は余分のエネルギーを光として放出する過程です。
2つ目は余分のエネルギーを熱として放出する過程です。
3つ目は余分のエネルギーを利用して化学反応を起こし別の化合物の基底状態になる過程です。
この最初の過程に伴って出される光を発光といいます。
この発光には2つの種類、すなわち「蛍光」と「りん光」があります。 「蛍光」は光っている時間が非常に短く(寿命が非常に短く)、「りん光」は光っている時間が長いため(寿命が長いため)発光体(光を出す物質)にあてている光を切っても、出てくる光をしばらくの時間見ることができる場合があります。このような光を残光といいます。 |
| |
a)蛍光とりん光 |
| |
「蛍光」と「りん光」の違いとして光っている時間の長さで区別しましたが、もう少し厳密に定義してみましょう。
「蛍光」は同じスピン多重度の状態間での発光、「りん光」は異なる多重度の状態間での発光ということができます。
通常の芳香族化合物などでは、「蛍光」は励起一重項状態から基底状態(これも一重項状態)への電子遷移にともなう発光です。それに対して、りん光は三重項状態から基底状態(一重項状態)への電子遷移に伴う発光です。一重項状態から一重項状態への遷移は電子のスピンがそのままの状態で起こります(電子のスピンの変化がない)ので、非常に短い時間で変化が起こります。それに対して、異なる項の間の遷移は電子のスピンが変化しなければならないため、本来禁制遷移です。そのため、この遷移が起こるためには長い時間が必要となります(寿命が長くなります)。
溶液中からの発光はほとんど「蛍光」です。三重項状態は寿命が長いため、溶液中に溶けている酸素などによって消光されるために、三重項状態は溶液中では非常に存在しにくいのです。
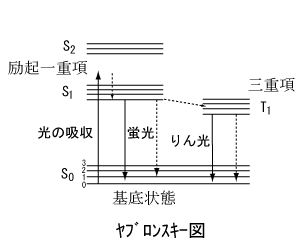 |
左の図はヤブロンスキー図(Jablonski
diagram)といわれているエネルギー状態の図です。S0、S1、S2はそれぞれ基底状態、第1励起一重項状態、第2励起一重項状態を表わしています。
また、T1は三重項状態を示しています。この図でもわかるように、一番低い一重項状態(第1励起一重項状態)からの発光が「蛍光」です。三重項状態からの発光が「りん光」となります。
これらの光を出してエネルギーの低い状態へ移る過程を輻射遷移といいます。 |
光を吸収して蛍光が出る様子を アニメで表わしたのが右の図です。
図の上にマウスのカーソルを置くと アニメが始まります。 |
|
|
| |
b)熱を放出する過程 |
| |
2つ目の「熱を放出する」過程は、光を出す過程と競争する過程です。上のヤブロンスキー図で点線で示した矢印の過程が熱を放出する過程を示しています。したがって、この過程が速く進むと蛍光などの発光効率が悪くなります。余分のエネルギーを熱エネルギーとして放出する過程を無輻射遷移といいます。
|
| |
c)化学反応を起こす過程 |
| |
3つ目の「余分のエネルギーを利用して化学反応を起こす」過程はいわゆる光化学反応です。通常の化学反応は熱エネルギーを駆動力として反応が起こります。そのため、温度を上げると反応の速さが増します。光化学反応は熱エネルギーよりはずっと大きい光のエネルギーを使うので、通常の熱反応では起こらないような反応が起こることがあります。 |
(2)化学発光について
ヤブロンスキー図における光の吸収過程の代わりに、化学発光では化学反応を利用します。化学反応に伴って発光体の励起状態が生じ、そこからの発光が起こります。化学発光での化学発光の原因となる化学反応としては酸化反応が一般的です。また、a)で述べたように、普通の条件下では三重項状態は存在しにくいために、化学発光で見られる発光は蛍光です。
ルミノールの化学発光は条件によって変わりますが、下の図のような反応機構が考えられています。 |
この図で * 印は励起状態にあることを示しています。また、2番目の反応式でのhν は光が出ていることを表わしており、この場合は蛍光が出ていることを意味しています。
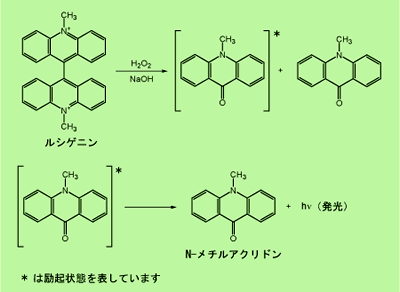
ルシゲニンもルミノール同様、自身が反応することにより、発光します。この反応は過酸化水素による酸化反応ですが、反応機構は複雑なようです。発光は生成した励起状態の
N-メチルアクリドンと考えられています。 |
| 過シュウ酸エステル化学発光の反応については「実験」の項目中で説明してあります。 |
|
■ X線
X 線は電磁波の仲間です。
■芳香族化合物
ベンゼン環をもつ炭素と水素からなる化合物をいいます。
■スピン多重度
電子が自転しているとすると右回りと左回りの回転があります。こ
■電子遷移
エネルギー状態で表わされるレベル(状態)は分子に含まれている電子のエネルギーレベルです。
■禁制遷移
遷移が理論的に起こりえないものを禁制遷移といいます。
■消光
他の分子(異なった種類あるいは同じ種類の物質でもかまいません)との衝突によって励起状態が基底状態へ変化させられることを消光といいます。
■Jablonski
Alexander Jablonski(ヤブロンスキー)は1898年生まれのポーランドの科学者 。 |
|





