通常、「電池」と聞くと自動車用のバッテリー(鉛蓄電池)やビデオカメラ、デジカメ、携帯電話などに使われているニッケル水素電池やリチウム電池などや、一般の機器に使われている種々の乾電池などを思い浮かべることが多いでしょう。これらの電池は電池内部に蓄えてある物質を化学反応させて電気エネルギーを取り出す仕組みになっています。そのため、それらの物質が化学反応によって変化してしまうと、それ以上電気エネルギーを取り出すことができなくなります。
燃料電池はこれらの電池と異なり、反応物質を外から連続的に供給し内部で化学反応させることによって、電気エネルギーを直接取り出すことができるのです。燃料電池に用いる反応物質は水素と酸素で、反応の結果水ができます。水素と酸素から水ができるということは、原料と生成物だけを見ると、水素を燃料とした燃焼と同じことになります。そこでこの装置を燃料電池とよびます。ただしここでは、普通の意味の燃焼が起きているわけではもちろんありません。仮に水素ガスと酸素ガスを混ぜて点火し燃焼させれば、爆発が起こり、エネルギーは熱や光や音に変わってしましますが、燃料電池という装置を使うことによって、それを電気エネルギーの形に少しずつ変えことができるというわけです。
反応物質として水素と酸素を使い、水が生成するだけで有害な物質が発生しないので、燃料電池はクリーンなエネルギー源として注目されています。燃料電池はまた、化学反応のエネルギーを直接電気エネルギーに変換するため、エネルギー変換の効率が高くなります。
火力発電所などでは石油や石炭を燃やしてでる熱エネルギーで水蒸気を作り、その力により発電機のタービンを回転させて機械エネルギーに変えます。さらにこの機械エネルギーを電気エネルギーに変えています。このように、何度もエネルギーの種類を変換することによるエネルギーのロスが生じます。
一方、燃料電池では化学反応のエネルギーを直接電気エネルギーに変えるためにエネルギーの変換効率が高くなります。
燃料電池で起こる化学反応は、いわば水の電気分解の逆の反応です。水の電気分解では電気エネルギーを加えることにより、水が電極上で水素と酸素になります。燃料電池では逆に水素と酸素から水が生成し、そのとき発生する化学反応のエネルギーを電気エネルギーとして取り出すことになります。
|
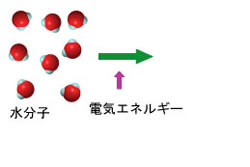 |
マウスのカーソルを左図の上に持っていくと、水の電気分解について模式的に示した反応を見ることができます。
|
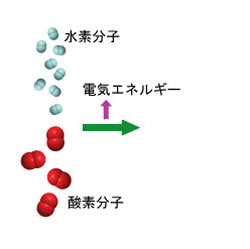 |
マウスのカーソルを左図の上に持っていくと燃料電池で起こる反応の模式的な様子を見ることができます。
この図は水素と酸素から水が生成し、そのとき発生するエネルギーを電気として取り出す燃料電池の原理を示しています。
|
燃料電池の種類としては、
(1)アルカリ形、
(2)固体高分子形、
(3)リン酸形、
(4)溶融炭酸塩形、
(5)固体酸化物形があります。
溶融炭酸塩形や固体酸化物形では常温で固体の物質を液化させて使うために、反応温度として数100度という高温が必要になります。それに対して、固体高分子形などでは室温付近などの比較的低い温度で電池を働かせることができます。
|
| (1) |
アルカリ形では高純度の水素が必要です。作動温度はおよそ100℃、電解質としてKOH水溶液を用います |
| (2) |
固体高分子形では水素を用い、温度は室温〜100℃程度、陽イオン交換膜を用います。 |
| (3) |
リン酸形では水素を用い、動作温度はおよそ200℃程度で、電解質としてリン酸を用います。 |
| (4) |
溶融炭酸塩形では水素を用い、動作温度は600〜700度程度です。電解質としては溶解したLi2CO3とK2CO3などが用いられます。 |
| (5) |
固体酸化物形では水素を用い、動作温度は900〜1000℃です。電解質としては溶解したZrO2などが用いられます。
|
|
■鉛蓄電池
電気を取り出すときの鉛蓄電池全体の化学反応は下の式で表わされます。
Pb + 2H2SO4 + PbO2 ----> 2PbSO4
+ 2H2O
■ニッケル水素電池
電極で反応する物質としてニッケル化合物(NiOOH)と水素を用いた電池です。
■リチウム電池
リチウム(Li)を電極物質として用いる電池です。
■アルカリ
水に溶けると酸とは反対の性質を示す物質をいいます。
■リン酸
H3PO4で表わされる、潮解性のある物質で水に容易にとけます。
■電解質
水などに溶けて溶液がイオン伝導性を示す物質を電解質といいます。 |
|





